一种针对胰腺癌固有屏障按需递释药物的纳米制剂及制备方法和应用
本发明属于药物制剂,涉及一种针对胰腺癌固有屏障按需递释药物的纳米制剂及制备方法和应用。
背景技术:
1、胰腺导管腺癌(pdac)恶性程度极高,临床上,作为抗肿瘤常规疗法或者术后辅助疗法的放化疗手段对pdac的治疗至关重要,但其总体疗效欠佳。与此同时,免疫疗法近年来在癌症治疗上取得了重大成功,但对于pdac患者,多个临床实践证明免疫疗法的抗pdac治疗收益不佳。
2、研究表明,pdac肿瘤微环境由细胞和细胞外基质成分组成,体积占比超80%的固有屏障是导致其化疗和免疫治疗效果不佳的主要原因。肿瘤相关成纤维细胞(cafs)大量分泌的胶原蛋白、纤维蛋白构成致密的细胞外基质(ecm),其通过不断压迫肿瘤微环境血管造成瘤内高间质液压和血管畸形,阻碍了治疗药物的血管渗透和肿瘤蓄积,造成耐药,被称为基质物理屏障。同时,致密ecm和部分细胞因子还会阻碍适应性免疫细胞(如细胞毒性t细胞)和nk细胞等杀伤性免疫细胞的肿瘤募集和浸润,最终形成免疫抑制屏障,以致新兴免疫疗法对pdac疗效不佳。
3、针对pdac固有屏障特征,多种已有的直接消融ecm的策略并未显著改善患者生存期,反而一定程度促进了pdac的转移。其表明ecm在pdac进展中具有矛盾的两面性作用:它不仅是影响药物治疗效果的耐药屏障,还是限制肿瘤细胞迁移和侵袭的保护屏障。这种困境挑战了从外部消除ecm的策略,并提出了从pdac病理特征出发治疗pdac的递药系统需求:不破坏ecm的前提下改善pdac固有屏障,协同给予化疗药物穿透固有屏障进行抗肿瘤治疗。
4、智能药物递送系统具有多模块、模块化、整体性、响应性等优良属性,具体表现为:(1)能够通过共价连接、疏水作用或者静电作用实现药物的高效、稳定荷载;(2)通过靶向功能基团修饰,能够增加靶细胞表面分子亲和力,从而实现肿瘤细胞的靶向摄取和蓄积;(3)能够响应肿瘤微环境低ph值、高ros和gsh、乏氧等微环境特征,迅速释放药物,实现目标受体的肿瘤特异性、高效抑制。因此,基于智能药物递送系统的药物共递送方案可能是针对胰腺癌固有屏障按需递释药物的有效策略。
技术实现思路
1、本发明为了实现上述目的,针对胰腺癌固有屏障,提供了一种能够按需递释药物,调控pdac固有屏障并进行抗肿瘤治疗的纳米制剂的制备方法和应用。本发明选择聚乙二醇-聚精氨酸-聚赖氨酸-硝基咪唑(peg-parg-plys-ni,pal-ni)作为构建胶束的基本单元。该聚合物片段能够通过聚精氨酸的正电性吸附吉西他滨单磷酸酯,这是化疗药物吉西他滨的活化形式。
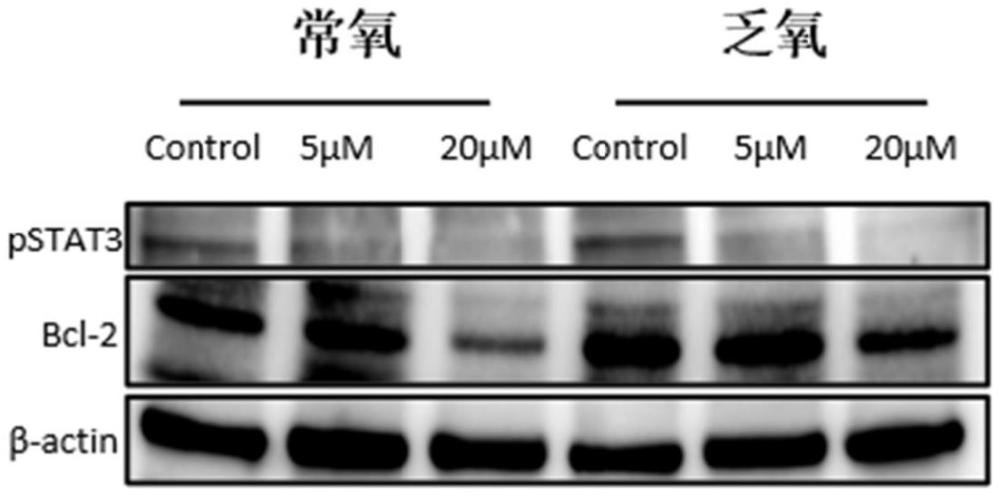
2、信号转导因子和转录激活因子3(stat3)分子在pdac的进展中起关键作用。stat3通路的激活能促进肿瘤细胞的增殖和转移,介导胰腺间质细胞形成ecm并参与免疫抑制微环境的构建。因此,广泛抑制肿瘤微环境中的stat3分子磷酸化,增强化疗药物诱导细胞凋亡的能力,重塑ecm和免疫环境是调控pdac固有屏障的有效手段。
3、该胶束可以利用疏水包封作用来负载stat3抑制剂水飞蓟宾。为了提高胶束的循环稳定性和肿瘤蓄积能力,在胶束的表面涂覆了透明质酸,得到透明质酸包被的载药纳米制剂。
4、表面呈电负性的纳米制剂在体内稳定循环,当到达肿瘤部位时,其表面的透明质酸可以与肿瘤细胞表面的cd44分子结合,实现肿瘤区域纳米颗粒的富集,并使胶束表面电荷翻正。当正电胶束处于肿瘤的缺氧区时,聚合物片段中的疏水性硝基咪唑基团会被硝基咪唑还原酶还原为亲水性基团,促进胶束的瓦解。此时,水飞蓟宾在肿瘤微环境中释放并广泛调控stat3信号,调控pdac固有屏障,而吉西他滨单磷酸酯附着正电性的聚合物片段深入肿瘤内部杀死肿瘤细胞。
5、具体地,本发明涉及一种针对胰腺癌固有屏障按需递释药物的纳米制剂,尤其涉及一种可以穿透肿瘤致密基质,实现化疗增敏,重塑ecm,逆转免疫抑制微环境从而提高对pdac抗肿瘤疗效的智能化纳米给药系统。
6、为实现上述目的,本发明提供的技术方案如下:
7、本发明提供一种针对胰腺癌固有屏障按需递释药物的纳米制剂,由结构简式如式ⅰ所示的聚合物peg-parg-plys-ni制备的胶束包载水飞蓟宾,静电吸附吉西他滨单磷酸酯并包覆透明质酸构成。
8、
9、优选的,hplc测得,所述纳米制剂对于吉西他滨单磷酸酯的载药量为4.7%,水飞蓟宾的载药量为8.6%;所述纳米制剂的平均粒径为59.19±1.63nm,zeta电位为-10.77±0.37mv。
10、本发明中,经核磁共振氢谱测试得到所述peg-parg-plys-ni中聚乙二醇链段、聚精氨酸链段、聚赖氨酸链段的重复单元数之比为1:11:21。
11、本发明还提供上述纳米制剂的制备方法,包括如下步骤:
12、通过薄膜水化法,将聚合物peg-parg-plys-ni与水飞蓟宾分散于有机溶剂中,旋蒸除去有机溶剂并形成薄膜,加入超纯水并超声分散得到胶束,胶束与吉西他滨单磷酸酯混合吸附后,再与透明质酸混合进行包覆,包覆后透析除去未包载的游离药得到纳米制剂。
13、优选的,所述peg-parg-plys-ni与水飞蓟宾、吉西他滨单磷酸酯、透明质酸的质量比为8:1:8:4;所述有机溶剂为dmf;所述超纯水与peg-parg-plys-ni的质量比为2000:1;所述超声分散的时间为2h;胶束与吉西他滨单磷酸酯的混合时间为1h;所述透明质酸包覆的时间为2h。
14、本发明还提供上述结构简式如式ⅰ所示的聚合物peg-parg-plys-ni的制备方法,包括以下步骤:
15、(1)将n6-苄氧羰基-l-赖氨酸与三光气按照fuchs-farthing法合成lys(cbz)-nca,反应温度为50℃;反应式如式ⅱ所示:
16、
17、(2)将boc-鸟氨酸与三光气按照fuchs-farthing法合成orn(boc)-nca,反应温度为50℃;反应式如式ⅲ所示:
18、
19、(3)将步骤(1)所得的lys(cbz)-nca与步骤(2)所得的orn(boc)-nca在无氧条件下于40-60℃与聚乙二醇进行开环聚合反应,得到peg-porn(boc)-plys(cbz);反应式如式ⅳ所示:
20、
21、(4)将步骤(3)所得的peg-porn(boc)-plys(cbz)于冰浴三氟乙酸环境中脱去boc保护基,反应式如式ⅴ所示;并于碱性条件下的水溶液中加入胍基化试剂进行胍基化反应,得白色固体peg-parg-plys(cbz);反应式如式ⅵ所示:
22、
23、(5)将步骤(4)所得的peg-parg-plys(cbz)于三氟乙酸/氢溴酸/醋酸环境中脱去cbz保护基,得peg-parg-plys,反应式如式ⅶ所示;
24、
25、(6)将2-羟甲基-1-甲基-5-硝基咪唑与缚酸剂、催化剂、对硝基苯基氯甲酸酯混合后于常温条件下反应,得白色固体pnp-ni,反应式如式ⅷ所示;
26、
27、(7)取步骤(6)中的pnp-ni、步骤(5)中的peg-parg-plys与缚酸剂、催化剂在室温下反应,得peg-parg-plys-ni,反应式如式ⅸ所示;
28、
29、优选的,步骤(1)中所述n6-苄氧羰基-l-赖氨酸与三光气的摩尔比为2.5:1;所述步骤(1)具体步骤为:将n6-苄氧羰基-l-赖氨酸和三光气加入反应瓶中,并通氩气进行保护;搅拌并加入溶剂无水四氢呋喃,于50℃下反应2h,反应结束后将反应液温度恢复至室温;边搅拌边将反应液滴入-20℃预冷的正己烷中;抽滤得到白色固体,即为lys(cbz)-nca。
30、优选的,步骤(2)中,boc-鸟氨酸与三光气按照fuchs-farthing法合成orn(boc)-nca,所述boc-鸟氨酸与三光气的摩尔比为2.5:1;所述步骤(2)具体步骤为:将boc-鸟氨酸和三光气加入反应瓶中,并通氩气进行保护;搅拌并加入溶剂无水四氢呋喃,于50℃下反应0.5-1h,反应结束后将反应液温度恢复至室温;边搅拌边将反应液滴入-20℃预冷的正己烷中;抽滤得到orn(boc)-nca。
31、优选的,步骤(3)中聚乙二醇、orn(boc)-nca、lys(cbz)-nca的摩尔比为1:(10~13):(18~22),所述聚乙二醇为ch3o-peg-nh2,重复单元数为112;步骤(3)具体步骤为:将ch3o-peg-nh2置于反应瓶中,加入orn(boc)-nca,通氩气保护后,加入溶剂无水dmf,于40-60℃下反应48h;而后加入lys(cbz)-nca,继续反应48h;反应结束后将反应液转移至透析袋中,于去离子水中透析24h,换两次水;之后将透析袋中的液体冷冻干燥,得白色固体peg-porn(boc)-plys(cbz)。
32、优选的,步骤(4)中的peg-porn(boc)-plys(cbz)与胍基化试剂的摩尔比为1:20;所述的胍基化试剂为3,5-二甲基吡唑-1-甲脒硝酸盐,碱性条件的ph值为9.3。
33、进一步优选的,步骤(4)中,peg-porn(boc)-plys(cbz)脱去boc保护基的方法:将1.5g的peg-porn(boc)-plys(cbz)加入40ml dcm和tfa的混合溶剂中,dcm:tfa体积比为1:1,冰浴下搅拌反应20min,并通过减压旋蒸除去溶剂;步骤(4)中所述的胍基化反应的具体步骤为:加入0.476g的3,5-二甲基吡唑-1-甲脒硝酸盐和90ml水,用naoh溶液将反应体系ph调至9.3后于37℃反应48h,之后将反应液转移至透析袋中,于去离子水中透析48h,换四次水,经冷冻干燥得白色固体peg-parg-plys(cbz)。
34、优选的,步骤(5)中,将1g的peg-parg-plys(cbz)于冰浴条件下加入40ml tfa和2ml氢溴酸/醋酸(hbr/hoac,33%,v/v)的混合溶液中,并在冰浴下反应3h后于去离子水中进行透析24h,换四次水;之后冷冻干燥得到白色固体peg-parg-plys。
35、优选的,所述步骤(6)和步骤(7)中的缚酸剂均为三乙胺,所述催化剂均为4-二甲胺基吡啶。
36、进一步优选的,步骤(6)中2-羟甲基-1-甲基-5-硝基咪唑与三乙胺、4-二甲胺基吡啶、对硝基苯基氯甲酸酯的摩尔比为1:(1.3~1.5):(0.005~0.02):(1.3~1.8);所述步骤(6)具体步骤为:将2-羟甲基-1-甲基-5-硝基咪唑、三乙胺和4-二甲胺基吡啶溶于无水thf中得到混合液;将对硝基苯基氯甲酸酯的四氢呋喃溶液,在2h内缓慢滴加至所述混合液中;之后于室温下反应10h;反应结束后加入硅胶粉,减压旋蒸除去溶剂,通过柱层析纯化得到白色固体pnp-ni,柱层析流动相为体积比(4-1):1的石油醚/乙酸乙酯混合液。
37、进一步优选的,步骤(7)中peg-parg-plys与三乙胺、4-二甲胺基吡啶、pnp-ni的摩尔比为1:(20~25):(0.1~0.3):(20~22);所述步骤(7)的具体步骤为:将peg-parg-plys、et3n、dmap和pnp-ni溶于dmf后得到反应液,反应液于室温下搅拌反应12h后转移至透析袋中,于dmf中透析24h,换一次dmf,再于去离子水中透析24h,换两次水,冷冻干燥后得到绿色固体peg-parg-plys-ni。
38、本发明还提供上述纳米制剂在制备抗胰腺癌药物中的应用。
39、本发明与现有技术相比,具有以下有益效果:
40、(1)本发明所述的纳米制剂在体内能长期并稳定循环,具有明显的实体瘤蓄积能力,可以将药物有效递送至肿瘤部位。
41、(2)本发明中的聚合物片段以聚乙二醇、氨基酸、硝基咪唑为骨架,结合对人体低毒的水飞蓟宾与生物相容性良好的透明质酸构建递送系统,降低了纳米载体引入系统毒性的风险。
42、(3)本发明所述的纳米制剂可以响应肿瘤微环境中的乏氧条件,按需将stat3抑制剂释放在肿瘤微环境中,将化疗药物递送到肿瘤深层,通过多靶点联合调控实现化疗增敏、重塑肿瘤基质、逆转免疫微环境,从而提高抗肿瘤疗效。
技术研发人员:蒋晨,李楚枫,孙涛
技术所有人:复旦大学
备 注:该技术已申请专利,仅供学习研究,如用于商业用途,请联系技术所有人。
声 明 :此信息收集于网络,如果你是此专利的发明人不想本网站收录此信息请联系我们,我们会在第一时间删除
