表达hTim4的登革出血热动物模型的应用的制作方法
本发明涉及疾病和药物研究,特别是涉及一种表达htim4的登革出血热动物模型的应用。
背景技术:
1、登革热疫情由登革热病毒(denv)引起,被认为是影响热带和亚热带地区人群的最重要的节肢动物传播的病毒感染之一。登革热疫情在全球范围内的持续传播可归因于气候突变、快速无计划的城市化和建设、高人口密度以及无效的媒介控制策略。科学界必须加强对解决这一持续的登革热流行病的关注。
2、登革热感染有四种常见的血清型,即denv-1至denv-4。2007年在马来西亚发现了一种新的血清型denv-5。感染登革热病毒的个体可以无症状或出现轻度登革热、神经系统并发症,也可以出现严重症状,如登革出血热(dhf)和登革休克综合征(dss),这些症状可能危及生命。重症登革热的特点是全身性出血倾向、血小板减少症、毛细血管渗漏、器官衰竭、休克,偶尔死亡。同一血清型感染可赋予终身免疫。然而,只能维持对异源感染的短期免疫,甚至可能在其他血清型感染时由于抗体依赖性增强(ade)而导致严重的登革热。抗击登革热流行的主要挑战包括对其发病机制和抗体依赖性增强(ade)的不清楚了解,以及缺乏特定的治疗方案和无效的预防疫苗。这些问题的解决,依赖于能有效模拟登革热疾病的动物模型。
3、目前,只有两种登革热疫苗dengvaxia和qdenga获得批准。这两个疫苗都是减毒活疫苗。减毒疫苗要满足低毒、低剂量、高免疫的特点。dengvaxia疫苗利用icr乳鼠进行安全性评价,用食蟹猴模型进行免疫原性和保护性评价,但食蟹猴缺乏显著的登革热临床表现,icr乳鼠感染登革病毒后,虽然可产生病毒血症,中和性抗体,但受限于自身免疫系统不健全和缺乏人类登革热的典型症状,也因此dengvaxia疫苗接种后可能严重不良事件。qdenga疫苗于2022年8月在印度尼西亚获得许可,随后在欧洲获得批准。然而,关于它们的预防功效和安全性的长期数据仍然是必要的。qdenga是用目前被广泛使用的干扰素i和ii型受体缺陷型小鼠ag129小鼠进行评价的。尽管在登革病毒感染ag129小鼠后,会观察到强烈的病毒血症、强烈的免疫反应、严重的登革热症状,甚至致命的感染,但ag129小鼠模型有几个局限性:(a)高度依赖适应菌株;(b)小鼠因中枢神经系统感染死亡;(c)缺乏自然免疫反应,从而影响疫苗研究的适宜性;(d)ifn信号通路阻断后的细胞因子风暴。
4、其他的登革热病毒感染模型,科学家们也进行了很多尝试,但都存在不同的局限性。恒河猴和树鼩表现出较低的病毒血症水平,而帽猴、狨猴、黑猩猩和尤卡坦迷你猪则没有明显的临床表现。因此建立一个免疫功能正常的,可模拟登革病毒感染导致的全身出血、器官衰竭和免疫风暴,有良好的ade反应的感染模型至关重要。
5、小鼠模型在模式生物中所具有的独特综合优势,不仅表现在遗传学与生理学上与人具有相似性,也有其成本低、繁殖饲养快速方便、遗传背景明确、以及相应基因编辑技术成熟等有利因素,使其成为新发突发传染病领域疾病模型、药物研发评价和疫苗研发评价研究等最为重要的模式动物。小鼠疾病模型的构建,可帮助人们深入揭示病毒感染致病机制,为临床前评价研究提供工具,是疫苗和药物研发基础研究向临床预防和治疗应用有效转化的重要桥梁。
技术实现思路
1、针对目前缺乏一种能够用于登革出血热发病机理及疫苗研发评价方法的问题,本发明提供一种表达htim4的登革出血热动物模型的应用,以该表达htim4的登革出血热动物模型对登革出血热进行研究,以及对其预防及治疗所用疫苗/药物进行研发和评价,可得到较好的评价结果。
2、本发明公开了一种表达htim4的登革出血热动物模型在筛选和/或评价用于治疗和/或预防登革出血热的药物,或在研究登革出血热病症机理中的应用,所述表达htim4的登革出血热动物模型为高表达人源tim4的小鼠,引发所述登革出血热症状的病毒为登革热病毒。
3、在其中一些实施例中,所述登革热病毒为denv-2病毒。
4、在其中一些实施例中,所述小鼠为c57bl/6小鼠。
5、在其中一些实施例中,所述药物为疫苗或感染体恢复体血清。例如,所述疫苗为登革热病毒减活疫苗。
6、在其中一些实施例中,所述表达htim4的登革出血热动物模型通过以下方法建立得到:
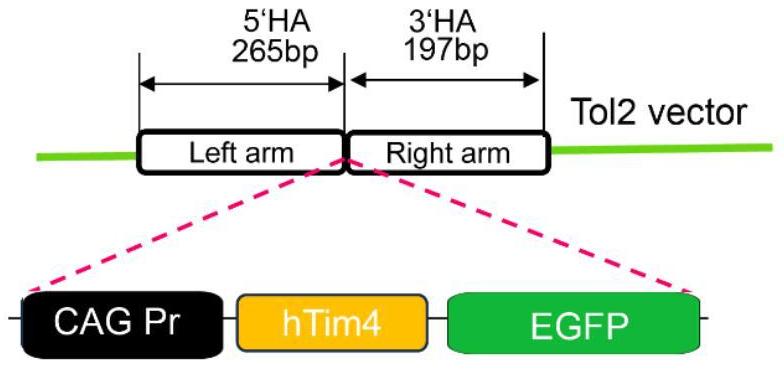
7、打靶载体构建:构建含人源tim4的dna片段的打靶载体;
8、培育f0代小鼠:将阳性打靶载体和编码tol2酶的载体注射入小鼠受精卵细胞中,并将存活的受精卵移植至假孕小鼠体内,筛选出生幼鼠中的阳性小鼠,即为f0代小鼠,备用;
9、繁育:将上述f0代小鼠与野生型同品系小鼠交配,得到表达htim4的小鼠为阳性小鼠;
10、感染:向所述阳性小鼠颅内注射登革病毒,即得所述登革出血热动物模型。
11、在其中一些实施例中,所述感染步骤中,所述登革病毒的注射剂量为为103tcid50/ml,每只小鼠颅内注射30±10微升。
12、在其中一些方案中,所述打靶载体含cag-kozak-htim4-p2a的序列片段,进一步地,所述打靶载体含cag-kozak-htim4-p2a-wpre的序列片段,更进一步地,所述打靶载体含cag-kozak-htim4-p2a-wpre-polya的序列片段。
13、可以理解的,上述cag、kozak、p2a、wpre、polya等序列片段,在打靶载体中所起的作用分别为基因表达的启动子、提高蛋白质的翻译、蛋白剪切、通过转录后调控机制增强目的基因表达和增加rna的稳定性、提高翻译效率等作用,也可根据本领域的通常用法,选择不同的功能基因片段,仅需确保后续转入的htim4基因能够稳定遗传和过表达即可。
14、在其中一些方案中,所述打靶载体含cag-kozak-htim4-p2a-egfp的序列片段,进一步地,所述打靶载体含cag-kozak-htim4-p2a-egfp-wpre的序列片段,更进一步地,所述打靶载体含cag-kozak-htim4-p2a-egfp-wpre-polya的序列片段。
15、可以理解的,上述egfp序列片段可编码环境敏感绿色荧光蛋白,可用于后续作为阳性小鼠筛选的标识,从模型本身功能而言,其并非是必须的。
16、在其中一些方案中,所述htim4的dna序列如seq id no:1所示。
17、在其中一些方案中,所述cag的序列如seq id no:2所示。
18、在其中一些方案中,所述kozak的序列为gccacc。
19、在其中一些方案中,所述p2a的序列如seq id no:3所示。
20、在其中一些方案中,所述egfp的序列如seq id no:4所示。
21、在其中一些方案中,所述wpre的序列如seq id no:5所示。
22、在其中一些方案中,所述polya的序列如seq id no:6所示。
23、在其中一些方案中,所述打靶载体序列如seq id no:7所示。
24、在其中一些方案中,所述载体为tol2载体。
25、可以理解的,上述tol2载体也被称为转座子质粒,包含两个反向末端重复序列(itrs)以及两者之间的转座区域,人源tim4基因即克隆在此区域,其余设计参照常规设计即可。
26、在其中一些方案中,编码所述tol2酶的tol2序列如seq id no:8所示。
27、在其中一些方案中,所述编码tol2酶的载体序列如seq id no:15所示
28、在其中一些方案中,采用如seq id no:9-seq id no:10所示引物对筛选阳性小鼠。
29、在其中一些方案中,所述打靶载体含有egfp序列片段,以ct成像系统进行体内荧光检测筛选阳性小鼠或采用如seq id no:11-seq id no:12所示引物对筛选阳性小鼠。
30、另一方面,本发明还公开了一种筛选和/或评价用于治疗和/或预防登革出血热的药物的方法,包括以下步骤:
31、给药:取上述的应用中的所述表达htim4的登革出血热动物模型,分为对照组和实验组,实验组预先给予待筛选和/或评价的药物,对照组进行平行操作但不给与药物;
32、测定:收集评价指标,所述评价指标包括:体重、病毒载量、解剖脏器病症、生存周期、生化指标和中和性抗体中的至少一种;
33、评价:将对照组和实验组测定所得评价指标进行对比分析,获得筛选和/或评价结果。
34、在其中一些实施例中,所述评价指标中,所述解剖脏器病症的脏器包括:脑、肺、肠组织、心脏、肝脏和脾脏中的至少一种;
35、所述生化指标包括:血常规、凝血酶原、免疫细胞、细胞因子中的至少一种,进一步地,所述细胞因子包括:th1、th2、ifn-γ、il-5、il-6、il-9、il-10、mcp-1、mcp-1α、mcp-1β和rantes中的至少一个。
36、在其中一些实施例中,所述测定步骤中,收集病毒感染后15天内的评价指标。
37、另一方面,本发明还公开了一种研究登革出血热病症机理的方法,包括以下步骤:
38、分组:取上述的应用中的所述表达htim4的登革出血热动物模型,作为实验组,取未经登革热病毒感染的小鼠作为对照组;
39、测定:收集评价指标,所述评价指标包括:体重、病毒载量、解剖脏器病症、生存周期、生化指标和空间转录组基因测序中的至少一种;
40、研究评价:将对照组和实验组测定所得评价指标进行对比分析,通过实验组和对照组的差异,对登革出血热进行研究评价。
41、在其中一些方案中,所述分组中,所述对照组小鼠为表达htim4的阳性小鼠;
42、所述评价指标中,所述解剖脏器病症的脏器包括:脑、肺、肠组织、心脏、肝脏和脾脏中的至少一种;
43、所述空间转录组测序的基因包括:col1a2,col1a1,clu,ceacm1,col3a1,klk1,reg3g,reg3b,hbb-bs和neu1中的至少一个;
44、所述生化指标包括:血常规、凝血酶原、免疫细胞、细胞因子中的至少一种,进一步地,所述细胞因子包括:th1、th2、ifn-γ、il-5、il-6、il-9、il-10、mcp-1、mcp-1α、mcp-1β和rantes中的至少一个。
45、在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
46、本发明所用试剂和原料均市售可得。
47、本发明的积极进步效果在于:
48、本发明的表达htim4的登革出血热动物模型的应用,首先以tol2转基因系统将人源tim4基因对小鼠进行转基因处理,得到能够稳定遗传过表达人源tim4(htim4)的小鼠模型。该模型具有正常的免疫功能,且对denv-2感染具有高度的易感性,感染登革病毒2后,可模拟典型的dhf/dss特征,如全身出血、神经并发症、严重肠道功能障碍和死亡。该模型可通过病毒血症、多器官出血、中和性抗体情况等多方面对登革出血热进行全面评估,为疫苗等药物的研制和评价提供支持和辅助。
技术研发人员:范昌发,王誉雅,吴勇,杨远松,谷文达,刘甦苏,曹愿,吴曦,王三龙,杨艳伟,柳全明
技术所有人:中国食品药品检定研究院(国家药品监督管理局医疗器械标准管理中心、中国药品检验总所)
备 注:该技术已申请专利,仅供学习研究,如用于商业用途,请联系技术所有人。
声 明 :此信息收集于网络,如果你是此专利的发明人不想本网站收录此信息请联系我们,我们会在第一时间删除
