p53-Y220C选择性小分子重激活剂化合物、药物组合物及其用途的制作方法
本发明属于药物化合物领域,具体涉及p53-y220c选择性小分子重激活剂化合物、药物组合物及其用途。
背景技术:
1、肿瘤是一系列相关疾病的集合,其特征是肿瘤细胞不受控制地增殖,并可能转移到全身各处。肿瘤细胞增殖离不开原癌基因和抑癌基因,基因突变可导致二者异常激活或活性抑制,进一步促进不受控制的细胞分裂。tp53作为著名的抑癌基因,被称为“基因组卫士”。tp53属于p53样转录因子家族,包括三个成员tp53、tp63和tp73基因,分别编码p53、p63和p73三种蛋白质。它们结构相似:dna结合结构域几乎相同,均可与相似的dna特异性序列结合,调节相同基因和一些不同基因的转录;c端结构域在大小、序列和功能上各不相同,调节dna结合和转录,介导蛋白相互作用;n末端序列至少编码两个不同的转录激活结构域。同p53相似,p63也是一个关键的转录因子,通过诱导细胞凋亡以应答dna损伤,作用于颅骨、面部、四肢和中枢神经系统,参与全身鳞状细胞上皮的产生和再生。纤毛上皮细胞的产生则需要p73,作用于雄性生殖细胞、免疫系统、听力系统、气管、肺、中枢神经系统等。
2、p53抑癌因子主要分布于细胞核浆,作为细胞应激的感受器,可应答于多种细胞应激,包括紫外线辐射、缺氧、癌基因激活和dna损伤等。p53激活后以四聚体形式与特定的dna序列结合,介导下游的基因转录,通过多种机制抑制癌症进展,如包括调控细胞周期,凋亡,衰老,干细胞分化,代谢(降低糖合成),ros和线粒体,dna损伤修复等。p53可以激活参与上述途径的蛋白质,包括例如fas/apol、killer/dr5、bax、puma、noxa、bid、caspase-3、caspase6、caspase 7、caspase_8、caspase-9和p21。此外,p53还可以抑制多种基因的转录,包括c-myc、cyclin b、vegf、rad51、htert。
3、由于其在肿瘤抑制中的关键作用,tp53基因是人类癌症中最常发生突变的基因,近50%恶性肿瘤中存在p53突变。与其他抑癌基因如rb1,apc,pten等的突变相反,大多数tp53突变是错义突变,比例高达75%。错义突变大多位于p53的dna结合结构域,导致dna识别和结合所需的蛋白序列异常折叠。p53可能发生突变的氨基酸位点有很多,如vall43、hisl68、argl75、tyr220、gly245、arg248、arg299、phe270、arg273和arg282。相应地,可以废除野生型p53活性的p53突变包括,例如,r175h、y220c、g245s、r248q、r248w、r273h和r282h。这些p53突变既可以扭曲dna结合位点的结构,也可破坏其热力学稳定性。tp53突变后通过纯合子缺失(loss of homozygousity)的形式失去野生型p53的抑癌转录活性;通过杂合子缺失的形式表现为显性负性作用(dominant negative effects),以及功能获得性作用(gain of function)如增加与p63和p73的结合等特征,从而促进肿瘤发生发展。因此,突变的p53蛋白可以被看作是一组异质蛋白,具有不同程度的正常肿瘤抑制功能的丧失和致癌特性的获得(gof)。
4、尽管不同p53突变体的活性不同,tp53错义突变体可以看作为原癌基因,促进肿瘤迁移、耐药导致预后不良,从而成为药物开发的治疗靶点。其中,致癌的p53 y220c突变体展现出特别合适的小分子稳定剂开发的典型结构。它是在癌症中发现的第九大最常见的p53错义突变,全球每年约10万例新发癌症病例。tyr220突变为cys会在p53 dbd表面形成一个狭窄的疏水性裂缝,从而降低其热稳定性约为4kcal/mol。野生型p53是中等稳定的,在44℃熔化变性,而y220c突变蛋白在生理条件的体温下就迅速从折叠状态展开变性,有效地消除了p53野生型的抑癌信号并驱动肿瘤发生。重要的是,y220c突变引起的疏水性裂缝远离参与dna识别或蛋白质相互作用的p53蛋白表面,从而允许在不干扰其与天然dna底物结合的情况下开发小分子药物。y220c突变体是一种温度敏感突变体,在较低的温度下与dna结合,在体温下变性。当小分子化合物选择性地与p53-y220c突变体结合后,该化合物可以稳定y220c突变体,以减少p53蛋白质在体温下变性的可能性,将p53从未折叠状态转变为折叠状态,恢复p53的野生型构象及转录活性。
5、研究表明已有若干小分子可与y220c突变体的疏水裂隙结合,如pk083,pk7088,pk5196,pc14586等,但仍存在起效浓度较高,因此不能排除是否是脱靶(off-target)的作用。因此,仍需开发更优的小分子从而更特异的与y220c突变体结合,更好的恢复p53野生型的结构与转录活性,更有效的抑制肿瘤。
技术实现思路
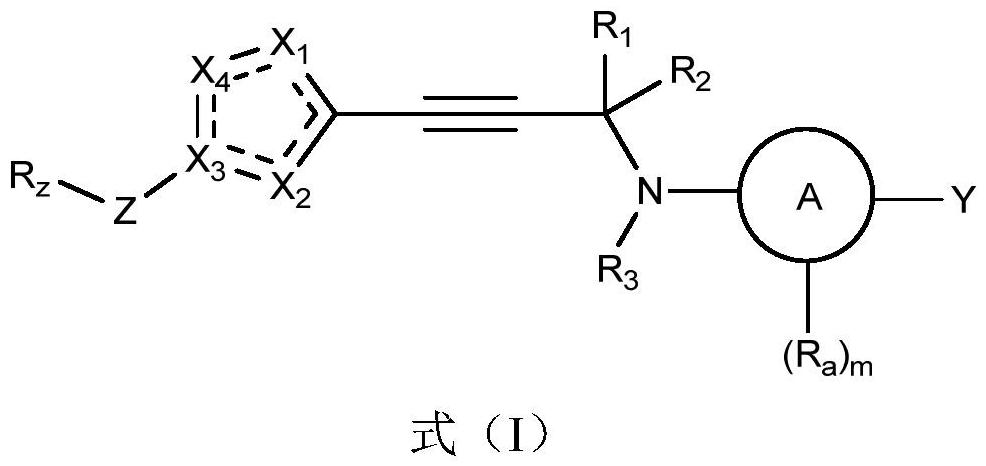
1、为解决现有技术中存在的问题,本发明提供一种式(i)所示的化合物及其消旋体、立体异构体、互变异构体、氮氧化物、溶剂化物、多晶型物、代谢产物、酯、前药或其药学上可接受的盐:
2、
3、其中,
4、r1、r2相同或不同,彼此独立地选自h、氘、卤素、c1-12烷基、c1-12烷氧基;
5、r3选自h、氘、c1-12烷基;
6、x1选自nrx11、crx12;
7、x2选自nrx21、crx22、o、s;
8、x4选自nrx41、crx42、o、s;
9、rx11、rx21、rx41不存在;或者rx11、rx21、rx41相同或不同,彼此独立地选自h、c1-12烷基、卤代c1-12烷基、c3-12环烷基;
10、rx12、rx22、rx42相同或不同,彼此独立地选自h、卤素、氰基、醛基、羧基、c1-12烷基、c2-12烯基、c1-12烷氧基、c3-12环烷基、卤代c1-12烷基、氰基c1-12烷基、卤代c2-12烯基、卤代c1-12烷氧基、卤代c3-12环烷基、-c(o)oc1-12烷基、-c(o)nh2;
11、x3选自c或n;
12、表示单键或双键;
13、环a选自c6-14芳环、5-14元杂芳环、3-14元杂环;
14、y不存在或者选自-c(=o)-ry1、-s(=o)-ry2、-s(=o)2-ry3、-p(=o)(ry4)(ry5)、-s(=o)(=nry6)-ry7、-c(=o)nh-ry8、ry9取代的5-14元杂芳基;ry1、ry2、ry3、ry4、ry5、ry6、ry7、ry8、ry9相同或不同,彼此独立地选自h、氘、无取代或任选被一个、两个或更多个ry取代的下列基团:c1-12烷基、c1-12烷氧基、c3-12环烷基、3-12元杂环基、卤代c1-12烷基、卤代c1-12烷氧基、c1-12烷基-nh-、(c1-12烷基)2n-、nh2;或者,ry4和ry5及其连接的p原子形成无取代或任选被一个、两个或更多个ry取代的3-14元杂环基;或者,ry6和ry7及其各自连接的原子形成无取代或任选被一个、两个或更多个ry取代的3-14元杂环基;或者,ry7与其连接的s原子形成与环a稠合的3-14元杂环基;
15、每个ry相同或不同,彼此独立地选自h、氘、卤素、氰基、c1-12烷基、c1-12烷氧基、c3-12环烷基、卤代c1-12烷基、卤代c1-12烷氧基、-c(=o)-c1-12烷基、-c(=o)-c3-12环烷基;
16、每个ra相同或不同,彼此独立地选自h、氘、氰基、卤素、氧代(=o)、无取代或任选被一个、两个或更多个ra1取代的下列基团:c1-12烷基、c1-12烷氧基、c3-12环烷基、oh、nh2;每个ra1相同或不同,彼此独立地选自h、氘、氰基、氧代(=o)、卤素、c1-12烷基、c1-12烷氧基、c3-12环烷基、卤代c1-12烷基、卤代c1-12烷氧基;
17、m选自0、1、2、3、4或5;
18、或者,y和一个ra与其各自连接的原子形成无取代或任选被一个、两个或更多个ra1取代的3-14元杂环基;
19、z不存在(即rz直接与x3键链)或者选自nh、o、s、ch2、ch2n(rz0)、c(o)nh;rz0选自h或c1-12烷基;
20、rz选自无取代或任选被一个、两个或更多个rz1取代的下列基团:c1-12烷基、c6-14芳基、5-14元杂芳基、3-14元杂环基、c3-12环烃基;每个rz1相同或不同,彼此独立地选自h、氘、oh、氰基、氧代(=o)、卤素、无取代或任选被一个、两个或更多个rz2取代的下列基团:ch2=、c1-12烷基、c1-12烷氧基、c3-12环烷基、3-14元杂环基、nh2;每个rz2相同或不同,彼此独立地选自h、氘、oh、氰基、氧代(=o)、卤素、无取代或任选被一个、两个或更多个rz3取代的下列基团:c1-12烷基、c1-12烷氧基、c3-12环烷基、3-14元杂环基、s(o)2c1-12烷基、nh2;每个rz3相同或不同,彼此独立地选自h、氘、oh、氰基、氧代(=o)、卤素、c1-12烷基、c1-12烷氧基、c3-12环烷基、c1-12烷基-nh-、(c1-12烷基)2n-、nh2。
21、根据一些实施方案,r1、r2、r3相同或不同,彼此独立地选自h、c1-6烷基。
22、根据一些实施方案,r1、r2、r3均为h。
23、根据一些实施方案,当x1选自nrx11时,x2选自crx22、n,x4选自crx42、n;当x1选自crx12时,x2选自n、o、s,x4选自n,s,o;
24、根据一些实施方案,rx11、rx21、rx41不存在;或者rx11、rx21、rx41相同或不同,彼此独立地选自h、c1-6烷基、c3-8环烷基、卤代c1-6烷基;rx12、rx22、rx42相同或不同,彼此独立地选自h、氰基、卤素、羧基、醛基、c1-6烷基、c2-6烯基、c3-8环烷基、卤代c1-6烷基、氰基c1-6烷基、卤代c2-6烯基、c3-8环烷基、-c(o)oc1-6烷基、-c(o)nh2;
25、根据一些实施方案,rx11、rx21、rx41不存在;或者rx11、rx21、rx41相同或不同,彼此独立地选自h、甲基、乙基、2-氟代乙基、2,2-二氟乙基、2,2,2-三氟乙基、环丙基、氰基;
26、根据一些实施方案,rx21、rx41不存在;rx11为2,2,2-三氟乙基。
27、根据一些实施方案,rx12、rx22、rx42相同或不同,彼此独立地选自h、甲基、乙基、f、cl、二氟甲基、氰基、氰基亚甲基、醛基、羧基、-c(o)och3、-c(o)nh2、2,2,2-三氟乙基、环丙基、乙烯基、
28、根据一些实施方案,rx12为2,2,2-三氟乙基;rx22选自h、甲基、乙基、f、cl、醛基、二氟甲基、氰基、氰基亚甲基、-c(o)och3、-c(o)nh2;rx42选自h、甲基、氰基、羧基、-c(o)och3、环丙基、乙烯基、
29、根据一些实施方案,环a选自c6-10芳环、5-10元杂芳环、5-10元杂环基;
30、根据一些实施方案,环a选自苯环、吡啶环、苯并噻吩环、苯并噻唑环、苯并呋喃环、2,3-二氢苯丙呋喃环。
31、根据一些实施方案,环a选自苯环、苯并噻吩环、苯并噻唑环、苯并呋喃环、2,3-二氢苯丙呋喃环。
32、根据一些实施方案,y选自-c(=o)-ry1、-s(=o)-ry2、-s(=o)2-ry3、-p(=o)(ry4)(ry5)、-s(=o)(=nry6)-ry7、-c(=o)nh-ry8、ry9取代的5-8元杂芳基;ry1、ry2、ry3、ry4、ry5、ry6、ry7、ry8、ry9相同或不同,彼此独立地选自h、无取代或任选被一个、两个或更多个ry取代的下列基团:c1-6烷基、c1-6烷氧基、c3-8环烷基、3-8元杂环基、卤代c1-6烷基、卤代c1-6烷氧基、c1-6烷基-nh-、(c1-6烷基)2n-、nh2;或者,ry4和ry5及其连接的p原子形成无取代或任选被一个、两个或更多个ry取代的3-6元杂环;
33、根据一些实施方案,每个ry相同或不同,彼此独立地选自h、卤素、氰基、c1-6烷基、c1-6烷氧基、c3-8环烷基、卤代c1-6烷基、卤代c1-6烷氧基、-c(=o)-c1-6烷基、-c(=o)-c3-8环烷基;
34、根据一些实施方案,ry1、ry2、ry3、ry4、ry5、ry6、ry7、ry8、ry9相同或不同,彼此独立地选自h、甲基、乙基、异丙基、环丙基、甲氨基、nh2、哌啶基、四氢吡喃基、哌嗪基、氰基甲基、2,2,2-三氟乙基;或者,ry4和ry5及其连接的p原子形成无取代或任选被一个、两个或更多个ry取代的
35、根据一些实施方案,每个ry相同或不同,彼此独立地选自h、f、氰基、甲基、乙基、甲氧基、环丙基、乙酰基、环丙甲酰基;
36、根据一些实施方案,y选自
37、根据一些实施方案,y和一个ra与其各自连接的原子形成无取代或任选被一个、两个或更多个ra1取代的3-8元杂环;例如
38、根据一些实施方案,每个ra相同或不同,彼此独立地选自h、氰基、卤素、无取代或任选被一个、两个或更多个ra1取代的下列基团:c1-6烷基、c1-6烷氧基、c3-8环烷基、oh、nh2;每个ra1相同或不同,彼此独立地选自h、氰基、氧代(=o)、卤素、c1-6烷基、c1-6烷氧基、c3-8环烷基、卤代c1-6烷基、卤代c1-6烷氧基;
39、根据一些实施方案,每个ra相同或不同,彼此独立地选自h、氰基、卤素、无取代或任选被一个、两个或更多个ra1取代的下列基团:c1-3烷基、c1-3烷氧基、c3-6环烷基、oh、nh2;每个ra1相同或不同,彼此独立地选自h、氰基、氧代(=o)、卤素、c1-3烷基、c1-3烷氧基、c3-6环烷基、卤代c1-3烷基、卤代c1-3烷氧基;
40、根据一些实施方案,每个ra相同或不同,彼此独立地选自氟、氯、甲氧基、三氟甲氧基、二氟甲氧基、一氟甲氧基、环丙基氧基、二氟甲基、三氟甲基、
41、根据一些实施方案,m选自1或2。
42、根据一些实施方案,m为1。
43、根据一些实施方案,环选自含有至少一个氮原子的五元杂芳环。本领域技术人员能够理解,该环中不应存在相邻的两个双键。
44、根据一些实施方案,环选自吡唑环、吡咯环、咪唑环、噻唑环、噁唑环。
45、根据一些实施方案,z不存在或者选自nh、o、s、ch2、ch2n(ch3)、c(o)nh、ch2nh。
46、根据一些实施方案,rz选自无取代或任选被一个、两个或更多个rz1取代的下列基团:c1-6烷基、5-10元杂环基、c5-10环烷基、c6-10芳基、5-10元杂芳基;
47、根据一些实施方案,rz选自无取代或任选被一个、两个或更多个rz1取代的下列基团:乙基、丙基、苯基、哌啶基、环己基、
48、根据一些实施方案,每个rz1相同或不同,彼此独立地选自氢、f、cl、甲基、甲氧基、氰基、氰基甲基、二甲氨基、氧代(=o)、氨基、甲氨基、乙氨基、二乙氨基、羟基、ch2=、chf=、cf2=、
49、根据一些实施方案,rz选自
50、
51、根据一些实施方案,式(i)所示的化合物具有如下所示的结构:
52、
53、其中,环a、y、z、ra、rz、r1、r2、r3、x1、x2、x3、x4、m具有本文中所述的定义。根据一些实施方案,式(i)所示的化合物具有如下所示的结构:
54、
55、其中,环a、y、z、ra、rz、r1、r2、r3、r11、r12、x2、x4、m具有本文中所述的定义。
56、根据一些实施方案,式(i)所示的化合物具有如下所示的结构:
57、
58、其中,y、z、ra、rz、r1、r2、r3、r11、r12、x2、x4、m具有本文中所述的定义。
59、根据一些实施方案,式(i)所示的化合物具有如下所示的结构:
60、
61、其中,z、rz、r1、r2、r3、r11、x2、具有本文中所述的定义。
62、根据一些实施方案,所述式(i)所示的化合物及其消旋体、立体异构体、互变异构体、氮氧化物、溶剂化物、多晶型物、代谢产物、酯、前药或其药学上可接受的盐中,式(i)所示的化合物的举例性的、非限制性的具体实例如下所示:
63、
64、
65、
66、
67、
68、
69、
70、
71、
72、
73、
74、
75、本发明还提供式(i)所示化合物的制备方法,包括以下步骤:
76、(1)化合物1与化合物2反应得到化合物3;
77、(2)化合物3与rz-zh反应得到式(i)所示化合物;
78、
79、环a、y、z、ra、rz、r1、r2、r3、x1、x2、x3、x4、m具有本文中所述的定义;l1和l2选自离去基团,如卤素,如l1选自br,l2选自br。
80、本发明还提供一种药物组合物,其包含治疗有效量的式(i)所示的化合物、其消旋体、立体异构体、互变异构体、氮氧化物、溶剂化物、多晶型物、代谢产物、酯、前药或其药学上可接受的盐中的至少一种。
81、根据本发明的实施方案,所述药物组合物还包括一种或多种药学上可接受的辅料。
82、根据本发明的实施方案,所述药物组合物还可以进一步含有一种或多种其他治疗剂。
83、本发明还提供一种治疗肿瘤疾病的方法,包括给予患者预防或治疗有效量的式(i)所示的化合物、其消旋体、立体异构体、互变异构体、氮氧化物、溶剂化物、多晶型物、代谢产物、酯、前药或其药学上可接受的盐中的至少一种。
84、根据本发明的实施方案,所述肿瘤为含有p53-y220c突变体的肿瘤。
85、本发明还提供治疗肿瘤疾病的方法,包括给予患者预防或治疗有效量的上述药物组合物。
86、在一些实施方案中,所述患者包括哺乳动物,优选是人。
87、本发明还提供用于治疗肿瘤疾病的式(i)所示的化合物、其消旋体、立体异构体、互变异构体、氮氧化物、溶剂化物、多晶型物、代谢产物、酯、前药或其药学上可接受的盐中的至少一种,或其药物组合物。
88、本发明还提供式(i)所示的化合物、其消旋体、立体异构体、互变异构体、氮氧化物、溶剂化物、多晶型物、代谢产物、酯、前药或其药学上可接受的盐中的至少一种在制备药物中的用途。
89、根据本发明的实施方案,所述用途可以为在制备抗含p53-y220c突变体的肿瘤药物中的用途,如在制备p53-y220c重激活剂药物中的用途。
90、根据本发明的实施方案,所述含p53-y220c突变体的肿瘤包括急性淋巴细胞白血病、急性髓细胞白血病、肾上腺皮质癌、艾滋病相关癌症、艾滋病相关淋巴瘤、肛门癌、阑尾癌、星形细胞瘤、基底细胞癌、胆管癌、膀胱癌、骨癌、脑肿瘤如小脑星形细胞瘤、大脑星形细胞瘤/恶性胶质瘤、室管膜瘤、髓母细胞瘤、幕上原始细胞瘤、神经外胚层肿瘤、视觉通路和下丘脑胶质瘤、乳腺癌、支气管腺瘤、伯基特淋巴瘤,未知原发癌,中枢神经系统淋巴瘤,小脑星形细胞瘤、宫颈癌、儿童癌症、慢性淋巴细胞白血病、慢性粒细胞性白血病、慢性骨髓增生性疾病、结肠癌、皮肤t细胞淋巴瘤、促纤维增生性小圆细胞瘤、子宫内膜癌、室管膜瘤、食管癌、尤因氏肉瘤、生殖细胞肿瘤、胆囊癌、胃癌、胃肠道类癌肿瘤、胃肠道间质肿瘤、胶质瘤、毛细胞白血病、头颈癌、心脏癌、肝细胞癌、霍奇金淋巴瘤、下咽癌、眼内黑色素瘤、胰岛细胞癌、卡波西肉瘤、肾癌、喉癌、唇癌和口腔癌、脂肪肉瘤、肝癌、肺癌如非小细胞肺癌和小细胞肺癌、淋巴瘤、白血病、巨球蛋白血症、恶性骨纤维组织细胞瘤/骨肉瘤、髓母细胞瘤、黑色素瘤、间皮瘤、转移性鳞癌伴隐性原发性、口腔癌、多发性内分泌肿瘤综合征、骨髓增生异常综合征、髓系白血病、鼻腔癌和鼻窦癌,鼻咽癌、神经母细胞瘤、非霍奇金淋巴瘤、非小细胞肺癌、口腔癌、口咽癌、骨肉瘤/骨恶性纤维组织细胞瘤、卵巢癌、卵巢上皮癌、卵巢生殖细胞瘤、胰腺癌、胰腺胰岛细胞癌、副鼻窦和鼻腔癌、甲状旁腺癌、阴茎癌、咽癌、嗜铬细胞瘤、松果体星形细胞瘤、松果体生殖细胞瘤、垂体腺瘤、胸膜肺母细胞瘤、浆细胞瘤、原发性中枢神经系统淋巴瘤、前列腺癌、直肠癌、肾细胞癌、肾盂和输尿管移行细胞癌、视网膜母细胞瘤、横纹肌肉瘤、唾液腺癌、肉瘤、皮肤癌、皮肤梅克尔细胞癌、小肠癌、软组织肉瘤、鳞状细胞癌、胃癌、t细胞淋巴瘤、喉癌、胸腺瘤、胸腺癌、甲状腺癌、滋养细胞肿瘤(妊娠期)、癌症原发部位未知,尿道癌,子宫肉瘤,阴道癌,外阴癌,瓦尔登斯特隆巨球蛋白血症和肾母细胞瘤。
91、有益效果
92、本发明的化合物具有良好的p53-y220c突变体激活作用,能够有效恢复p53-y220c突变蛋白的活性,用以治疗含p53-y220c突变蛋白的肿瘤疾病,以及制备用于此类病症或疾病的药物。
93、术语定义与说明
94、除非另有说明,本技术说明书和权利要求书中记载的基团和术语定义,包括其作为实例的定义、示例性的定义、优选的定义、表格中记载的定义、实施例中具体化合物的定义等,可以彼此之间任意组合和结合。这样的组合和结合后的基团定义及化合物结构,应当被理解为本技术说明书和/或权利要求书记载的范围内。
95、除非另有说明,本说明书和权利要求书记载的数值范围相当于至少记载了其中每一个具体的整数数值。例如,数值范围“1-14”相当于记载了数值范围“1-14”中的每一个整数数值,即1、2、3、4、5、6、7、8、9、10、11、12、13、14。
96、本技术通式定义中的术语“任选的”(或“任选地”、“任选”)意味着被零个、一个或多个取代基所取代的情形,例如“任选被一个、两个或更多个r取代”意味着可以不被r取代(无取代)或可以选择被一个、两个或更多个r取代。
97、“更多个”表示三个或三个以上。
98、术语“c1-12烷基”应理解为表示具有1~12个碳原子的直链和支链烷基,“c1-8烷基”表示具有1、2、3、4、5、6、7、或8个碳原子的直链和支链烷基,“c1-6烷基”表示具有1、2、3、4、5或6个碳原子的直链和支链烷基。所述烷基是例如甲基、乙基、丙基、丁基、戊基、己基、异丙基、异丁基、仲丁基、叔丁基、异戊基、2-甲基丁基、1-甲基丁基、1-乙基丙基、1,2-二甲基丙基、新戊基、1,1-二甲基丙基、4-甲基戊基、3-甲基戊基、2-甲基戊基、1-甲基戊基、2-乙基丁基、1-乙基丁基、3,3-二甲基丁基、2,2-二甲基丁基、1,1-二甲基丁基、2,3-二甲基丁基、1,3-二甲基丁基或1,2-二甲基丁基等或它们的异构体。
99、“c2-12烯基”应理解为优选表示直连或支链的一价烃基,其包含一个或多个双键并且具有2、3、4、5、6、7、8、9、10、11或12个碳原子,更优选“c2-8烯基”。“c2-8烯基”应理解为优选表示直连或支链的一价烃基,其包含一个或多个双键并且具有2、3、4、5、6、7或8个碳原子,例如,具有2、3、4、5或6个碳原子(即,c2-6烯基),具有2或3个碳原子(即,c2-3烯基)。应理解,在所述烯基包含多于一个双键的情况下,所述双键可相互分离或者共轭。所述烯基是例如乙烯基、烯丙基、(e)-2-甲基乙烯基、(z)-2-甲基乙烯基、(e)-丁-2-烯基、(z)-丁-2-烯基、(e)-丁-1-烯基、(z)-丁-1-烯基、戊-4-烯基、(e)-戊-3-烯基、(z)-戊-3-烯基、(e)-戊-2-烯基、(z)-戊-2-烯基、(e)-戊-1-烯基、(z)-戊-1-烯基、己-5-烯基、(e)-己-4-烯基、(z)-己-4-烯基、(e)-己-3-烯基、(z)-己-3-烯基、(e)-己-2-烯基、(z)-己-2-烯基、(e)-己-1-烯基、(z)-己-1-烯基、异丙烯基、2-甲基丙-2-烯基、1-甲基丙-2-烯基、2-甲基丙-1-烯基、(e)-1-甲基丙-1-烯基、(z)-1-甲基丙-1-烯基、3-甲基丁-3-烯基、2-甲基丁-3-烯基、1-甲基丁-3-烯基、3-甲基丁-2-烯基、(e)-2-甲基丁-2-烯基、(z)-2-甲基丁-2-烯基、(e)-1-甲基丁-2-烯基、(z)-1-甲基丁-2-烯基、(e)-3-甲基丁-1-烯基、(z)-3-甲基丁-1-烯基、(e)-2-甲基丁-1-烯基、(z)-2-甲基丁-1-烯基、(e)-1-甲基丁-1-烯基、(z)-1-甲基丁-1-烯基、1,1-二甲基丙-2-烯基、1-乙基丙-1-烯基、1-丙基乙烯基、1-异丙基乙烯基。
100、术语“c1-12烷氧基”应理解为“c1-12烷基-o-”,c1-12烷基如上所定义。
101、术语“c3-12环烃基”应理解为饱和或者部分饱和的一价单环、二环(如稠环、桥环、螺环)或三环烃基,其具有3~12个碳原子,优选“c3-10环烃基”,更优选“c3-8环烃基”。术语“c3-12环烃基”应理解为表示饱和或者部分饱和的一价单环、双环(如桥环、螺环)或三环烃基,其具有3、4、5、6、7、8、9、10、11或12个碳原子,所述碳原子是全部单键键链或者部分单键,部分双键和/或三键键链。所述c3-12环烃基可以是单环烃基,例如单环烷基,如环丙基、环丁基、环戊基、环己基、环庚基、环辛基、环壬基或环癸基,或者是双环烃基如龙脑基、四氢萘基、十氢萘基、二环[2.1.1]己基、二环[2.2.1]庚基、二环[2.2.1]庚烯基、6,6-二甲基二环[3.1.1]庚基、2,6,6-三甲基二环[3.1.1]庚基、二环[2.2.2]辛基、2,7-二氮杂螺[3,5]壬烷基、2,6-二氮杂螺[3,4]辛烷基,或者是三环烃基如金刚烷基。
102、术语“c3-12环烷基”应理解为饱和的一价单环、二环(如稠环、桥环、螺环)或三环烷基,其具有3~12个碳原子,优选“c3-10环烷基”,更优选“c3-8环烷基”。术语“c3-12环烷基”应理解为饱和的一价单环、双环(如桥环、螺环)或三环烷基,其具有3、4、5、6、7、8、9、10、11或12个碳原子,所述碳原子是全部单键键链。所述c3-12环烷基可以是单环烷基,如环丙基、环丁基、环戊基、环己基、环庚基、环辛基、环壬基或环癸基,或者是双环烷基如龙脑基、十氢萘基、二环[2.1.1]己基、二环[2.2.1]庚基、6,6-二甲基二环[3.1.1]庚基、2,6,6-三甲基二环[3.1.1]庚基、二环[2.2.2]辛基、2,7-二氮杂螺[3,5]壬烷基、2,6-二氮杂螺[3,4]辛烷基,或者是三环烃基如金刚烷基。
103、术语“c6-14芳基”应理解为优选表示具有6~14个碳原子的一价芳香性或部分芳香性的单环、二环或三环烃环,其可以是单芳族环或稠合在一起的多芳族环,优选“c6-10芳基”。术语“c6-14芳基”应理解为优选表示具有6、7、8、9、10、11、12、13或14个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环(“c6-14芳基”),特别是具有6个碳原子的环(“c6芳基”),例如苯基;或联苯基,或者是具有9个碳原子的环(“c9芳基”),例如茚满基或茚基,或者是具有10个碳原子的环(“c10芳基”),例如四氢化萘基、二氢萘基或萘基,或者是具有13个碳原子的环(“c13芳基”),例如芴基,或者是具有14个碳原子的环(“c14芳基”),例如蒽基。当所述c6-20芳基被取代时,其可以为单取代或者多取代。并且,对其取代位点没有限制,例如可以为邻位、对位或间位取代。
104、术语“5-14元杂芳基”应理解为包括这样的一价单环、二环(如稠环、桥环、螺环)或三环芳族环系:其具有5~14个环原子且包含1-5个独立选自n、o和s的杂原子,例如“5-10元杂芳基”。术语“5-14元杂芳基”应理解为包括这样的一价单环、双环或三环芳族环系:其具有5、6、7、8、9、10、11、12、13或14个环原子,特别是5或6或9或10个碳原子,且其包含1-5个,优选1-3各独立选自n、o和s的杂原子并且,另外在每一种情况下可为苯并稠合的。“杂芳基”还指其中杂芳族环与一个或多个芳基、脂环族或杂环基环稠合的基团,其中所述连接的根基或点在杂芳族环上。非限制性实例包括1-、2-、3-、5-、6-、7-或8-吲嗪基、1-、3-、4-、5-、6-或7-异吲哚基、2-、3-、4-、5-、6-或7-吲哚基、2-、3-、4-、5-、6-或7-吲唑基、2-、4-、5-、6-、7-或8-嘌呤基、1-、2-、3-、4-、6-、7-、8-或9-喹嗪基、2-、3-、4-、5-、6-、7-或8-喹啉基、1-、3-、4-、5-、6-、7-或8-异喹啉基、1-、4-、5-、6-、7-或8-酞嗪基(phthalazinyl)、2-、3-、4-、5-或6-萘啶基、2-、3-、5-、6-、7-或8-喹唑啉基、3-、4-、5-、6-、7-或8-噌啉基、2-、4-、6-或7-蝶啶基、1-、2-、3-、4-、5-、6-、7-或8-4ah咔唑基、1-、2-、3-、4-、5-、6-、7-或8-咔唑基咔唑基、1-、3-、4-、5-、6-、7-、8-或9-咔啉基、1-、2-、3-、4-、6-、7-、8-、9-或10-菲啶基、1-、2-、3-、4-、5-、6-、7-、8-或9-吖啶基、1-、2-、4-、5-、6-、7-、8-或9-啶基、2-、3-、4-、5-、6-、8-、9-或10-菲咯啉基、1-、2-、3-、4-、6-、7-、8-或9-吩嗪基、1-、2-、3-、4-、6-、7-、8-、9-或10-吩噻嗪基、1-、2-、3-、4-、6-、7-、8-、9-或10-吩嗪基、2-、3-、4-、5-、6-或1-、3-、4-、5-、6-、7-、8-、9-或10-苯并异喹啉基、2-、3-、4-或噻吩并[2,3-b]呋喃基、2-、3-、5-、6-、7-、8-、9-、10-或11-7h-吡嗪并[2,3-c]咔唑基、2-、3-、5-、6-或7-2h-呋喃并[3,2-b]-吡喃基、2-、3-、4-、5-、7-或8-5h-吡啶并[2,3-d]-邻-嗪基、1-、3-或5-1h-吡唑并[4,3-d]-唑基、2-、4-或54h-咪唑并[4,5-d]噻唑基、3-、5-或8-吡嗪并[2,3-d]哒嗪基、2-、3-、5-或6-咪唑并[2,1-b]噻唑基、1-、3-、6-、7-、8-或9-呋喃并[3,4-c]噌啉基、1-、2-、3-、4-、5-、6-、8-、9-、10或11-4h-吡啶并[2,3-c]咔唑基、2-、3-、6-或7-咪唑并[1,2-b][1,2,4]三嗪基、7-苯并[b]噻吩基、2-、4-、5-、6-或7-苯并唑基、2-、4-、5-、6-或7-苯并咪唑基、2-、4-、4-、5-、6-或7-苯并噻唑基、1-、2-、4-、5-、6-、7-、8-或9-苯并氧杂基(benzoxapinyl)、2-、4-、5-、6-、7-或8-苯并嗪基、1-、2-、3-、5-、6-、7-、8-、9-、10-或11-4h-吡咯并[1,2-b][2]苯并氮杂基(benzazapinyl)。典型的稠合杂芳基包括但不限于2-、3-、4-、5-、6-、7-或8-喹啉基、1-、3-、4-、5-、6-、7-或8-异喹啉基、2-、3-、4-、5-、6-或7-吲哚基、2-、3-、4-、5-、6-或7-苯并[b]噻吩基、2-、4-、5-、6-或7-苯并唑基、2-、4-、5-、6-或7-苯并咪唑基和2-、4-、5-、6-或7-苯并噻唑基。当所述5-14元杂芳基与其它基团相连构成本发明的化合物时,可以为5-14元杂芳基环上的碳原子与其它基团相连,也可以为5-14元杂芳基环上的杂原子与其它基团相连。当所述5-14元杂芳基被取代时,其可以为单取代或者多取代。并且,对其取代位点没有限制,例如可以为杂芳基环上与碳原子相连的氢被取代,或者杂芳基环上与杂原子相连的氢被取代。
105、除非另有定义,术语“3-14元杂环基”是指饱和的或不饱和的非芳族的环或环系,例如,其是4-、5-、6-或7-元的单环、7-、8-、9-、10-、11-或12-元的二环(如稠环、桥环、螺环)或者10-、11-、12-、13-或14-元的三环环系,并且含有至少一个,例如1、2、3、4、5个或更多个选自o、s和n的杂原子,其中n和s还可以任选被氧化成各种氧化状态,以形成氮氧化物、-s(o)-或-s(o)2-的状态。优选地,所述杂环基可以选自“3-10元杂环基”。术语“3-10元杂环基”意指饱和的或不饱和的非芳族的环或环系,并且含有至少一个选自o、s和n的杂原子。所述杂环基可以通过所述碳原子中的任一个或氮原子(如果存在的话)与分子的其余部分连接。所述杂环基可以包括稠合的或桥连的环以及螺环的环。特别地,所述杂环基可以包括但不限于:4元环,如氮杂环丁烷基、氧杂环丁烷基;5元环,如四氢呋喃基、二氢呋喃基、二氧杂环戊烯基、吡咯烷基、二氢吡咯烷基、咪唑烷基、吡唑烷基、吡咯啉基;或6元环,如四氢吡喃基、哌啶基、吗啉基、二噻烷基、硫代吗啉基、哌嗪基或三噻烷基;或7元环,如二氮杂环庚烷基。任选地,所述杂环基可以是苯并稠合的。所述杂环基可以是双环的,例如但不限于5,5元环,如六氢环戊并[c]吡咯-2(1h)-基环,或者5,6元双环,如六氢吡咯并[1,2-a]吡嗪-2(1h)-基环。“杂环基”还指其中杂环与一个或多个芳基、脂环族或杂环基环稠合的基团,其中所述连接的根基或点在杂环上。杂环基可以是部分不饱和的,即它可以包含一个或多个双键,例如但不限于二氢呋喃基、二氢吡喃基、2,5-二氢-1h-吡咯基、4h-[1,3,4]噻二嗪基、1,2,3,5-四氢噁唑基或4h-[1,4]噻嗪基,或者,它可以是与含有至少一个选自o、s和n的杂原子的5元环或6元环苯并稠合的,其中具体的5元环或6元环如上所述,具体的实例包括但不限于二氢异喹啉基、二氢苯并呋喃基、二氢苯并吡咯基。所述3-14元杂环基与其它基团相连构成本发明的化合物时,可以为3-14元杂环基上的碳原子与其它基团相连,也可以为3-14元杂环基环上杂环原子与其它基团相连。例如当3-14元杂环基选自哌嗪基时,可以为哌嗪基上的氮原子与其它基团相连。或当3-14元杂环基选自哌啶基时,可以为哌啶基环上的氮原子和其对位上的碳原子与其它基团相连。
106、术语“螺环”是指两个环共用1个成环原子的环系。
107、术语“稠环”是指两个环共用2个成环原子的环系。
108、术语“桥环”是指两个环共用3个以上成环原子的环系。
109、术语“卤素”表示氟、氯、溴和碘。
110、“卤代”指被一个或多个卤素取代。
111、在本发明中,所涉及的化合物亦包括经同位素标记的化合物,所述经同位素标记的化合物与式i中所示的那些相同,但是其中一或多个原子被原子质量或质量数不同于通常天然存在的原子质量或质量数的原子替代。可掺入本发明的化合物的同位素的实例包括h、c、n、o、s、f及cl的同位素,分别诸如2h、3h、13c、11c、14c、15n、18o、17o、32p、35s、18f及36cl。含有上述同位素和/或其他原子的其他同位素的本发明的化合物、其前药、或者所述化合物或所述前药的药学上可接受的盐在本发明的范围内。本发明的某些经同位素标记的化合物,例如掺入放射性同位素(诸如3h和14c)的化合物可用于药物和/或底物组织分布测定。氚(即3h)和碳14(即14c)同位素因易于制备和可检测性而成为特别优选的。再者,以较重的同位素(诸如氘,即2h或d)替代可提供源自更高的代谢稳定性的某些治疗优势(例如增加的体内半衰期或减少的剂量需求),并因此可在某些情况下是优选的。本发明取代基中出现的氢未单独列明术语氘或氚并不表示排除氘或氚,而是同样也可以包含氘或氚。
112、本发明所述化合物的化学结构中,键表示未指定构型,表示绝对构型,即如果化学结构中存在立体异构体,键可以为或者同时包含两种构型。
113、本领域技术人员可以理解,式(i)所示化合物可以以各种药学上可接受的盐的形式存在。如果这些化合物具有碱性中心,则其可以形成酸加成盐;如果这些化合物具有酸性中心,则其可以形成碱加成盐;如果这些化合物既包含酸性中心(例如羧基)又包含碱性中心(例如氨基),则其还可以形成内盐。
114、本发明的化合物可以溶剂合物(如水合物)的形式存在,其中本发明的化合物包含作为所述化合物晶格的结构要素的极性溶剂,特别是例如水、甲醇或乙醇。极性溶剂特别是水的量可以化学计量比或非化学计量比存在。
115、根据其分子结构,本发明的化合物可以是手性的,因此可能存在各种对映异构体形式。因而这些化合物可以以消旋体形式或光学活性形式存在。本发明的化合物涵盖了各手性碳为r或s构型的异构体或其混合物、消旋体。本发明的化合物或其中间体可以通过本领域技术人员公知的化学或物理方法分离为对映异构体化合物,或者以此形式用于合成。在外消旋的胺的情况中,通过与光学活性的拆分试剂反应,从混合物制得非对映异构体。适当的拆分试剂的示例是光学活性的酸,例如r和s形式的酒石酸、二乙酰酒石酸、二苯甲酰酒石酸、扁桃酸、苹果酸、乳酸、适当的n-保护的氨基酸(例如n-苯甲酰脯氨酸或n-苯磺酰基脯氨酸)或各种光学活性的樟脑磺酸。借助光学活性的拆分试剂(例如固定在硅胶上的二硝基苯甲酰基苯基甘氨酸、三乙酸纤维素或其它碳水化合物的衍生物或手性衍生化的异丁烯酸酯聚合物),也可有利地进行色谱对映体拆分。用于此目的的适当的洗脱剂是含水或含醇的溶剂混合物,例如,己烷/异丙醇/乙腈。
116、可以根据已知的方法,例如通过萃取、过滤或柱层析来分离相应的稳定异构体。
117、术语“患者”是指包括哺乳动物在内的任何动物,优选小鼠、大鼠、其它啮齿类动物、兔、狗、猫、猪、牛、羊、马或灵长类动物,最优选人。
118、术语“治疗有效量”是指研究人员、兽医、医师或其它临床医师正在组织、系统、动物、个体或人中寻找的引起生物学或医学反应的活性化合物或药物的量,它包括以下一项或多项:(1)预防疾病:例如在易感染疾病、紊乱或病症但尚未经历或出现疾病病理或症状的个体中预防疾病、紊乱或病症。(2)抑制疾病:例如在正经历或出现疾病、紊乱或病症的病理或症状的个体中抑制疾病、紊乱或病症(即阻止病理和/或症状的进一步发展)。(3)缓解疾病:例如在正经历或出现疾病、紊乱或病症的病理或症状的个体中缓解疾病、紊乱或病症(即逆转病理和/或症状)。
技术研发人员:耿开骏,陆标,杨方龙,王思勤,金磊
技术所有人:长春金赛药业有限责任公司
备 注:该技术已申请专利,仅供学习研究,如用于商业用途,请联系技术所有人。
声 明 :此信息收集于网络,如果你是此专利的发明人不想本网站收录此信息请联系我们,我们会在第一时间删除
